9月26日,中国国家药品监督管理局药品审评中心(CDE)官网新公示,由百时美施贵宝公司(BMS)旗下新基(Celgene)申报的1类新药mezigdomide(CC-92480)胶囊已获得临床试验默示许可,拟开发用于复发性或难治性多发性骨髓瘤(研究方案编号:CA057-001)。公开资料显示,这是BMS公司开发的蛋白降解疗法CELMoD分子,目前已在海外进入3期临床试验阶段。
截图来源:CDE官网
蛋白降解疗法CELMoD分子是BMS公司基于多发性骨髓瘤疗法泊马度胺和来那度胺开发的新型化合物。通常的药物开发顺序是从疾病出发,先发现靶点,再开发针对靶点的创新疗法。而CELMoD分子的开发顺序则反其道而行之,这些候选疗法的开发过程是先有针对靶点的化合物,然后再发现它们降解的蛋白靶点,找出与这些靶点相关的疾病。
研究人员发现,泊马度胺和来那度胺治疗多发性骨髓瘤的机制之一是,它们可以与E3泛素连接酶CRBN相结合,从而改变CRBN为不同蛋白靶点添加泛素标签的能力。而被加上泛素标签的蛋白将会被送到细胞内的蛋白酶体中降解,从而达到免疫调节和抗肿瘤的效果。因此,与泊马度胺和来那度胺功能相似的CELMoD分子能够通过与CRBN结合,提高不同靶点蛋白的降解。
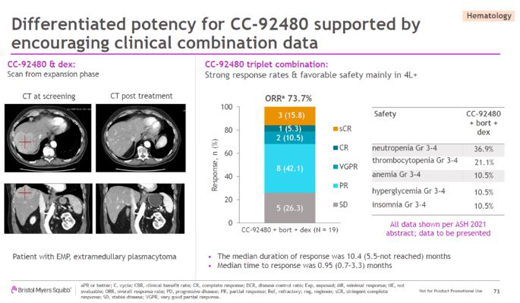
CC-92480正是一款在来那度胺基础上开发出的创新分子,它被设计为蛋白降解能力更强。在体外细胞培养实验中,研究人员发现,CC-92480降解Aiolos转录因子的能力越强,越能够迅速导致多发性骨髓瘤细胞系的死亡。此前,该产品已在1期临床试验中表现出更具差异化的临床活性。数据显示,它与两种其它标准疗法联用治疗难治性多发性骨髓瘤患者,达到73.7%的客观缓解率和10.4个月的中位缓解持续时间。
CC-92480的1期临床试验结果(图片来源:参考资料[1])
根据ClinicalTrials网站,目前CC-92480正在海外开展多项针对复发或难治性多发性骨髓瘤患者的临床试验,其中包括:一项比较CC-92480、硼替佐米和地塞米松(480Vd方案)与泊马度胺、硼替佐米和地塞米松(PVd方案)的3期临床试验;一项评估CC-92480单药治疗以及与地塞米松联合治疗的1/2期临床试验;一项评估CC-92480与标准治疗联合治疗的1/2期临床试验等。
多发性骨髓瘤是血液系统的第二常见恶性肿瘤,约占血液系统恶性肿瘤的10%。目前它仍然是一种无法治愈的血液癌症,几乎所有患者会出现复发并且需要接受后续治疗。随着疾病的进展,每次复发的侵袭性增强,而新疗法获得的缓解期逐渐缩短。因此,行业正在开发全新作用机制的创新疗法,从而满足尚未解决的临床需求。
声明:本文版权归原作者所有,转载文章仅为传播更多信息,如作者信息标记有误,或侵犯您的版权,请联系我们,我们将在及时修改或删除内容,联系邮箱:marketing@360worldcare.com